PRÁCTICAS CLÍNICAS, COSTOS, FINANCIAMIENTO Y ANÁLISIS DE COSTO-EFECTIVIDAD DE LA PROFILAXIS CON EMICIZUMAB PARA PACIENTES CON HEMOFILIA A E INHIBIDORES EN CHILE (Clinical practices costs, funding and cost-effectiveness analysis of emicizumab prophylaxis for patients with hemophilia A and inhibitors in Chile).
Ricardo Bitrán1, Paula Arpón1, Camila Peña1
1Bitrán & Asociados, Santiago
Lo Fontecilla 201, Oficina 433, Santiago, Chile 7550000
Tel. +569 9256 9862
ricardo.bitran@bitran.cl
Resumen
La hemofilia A es una patología causada por una deficiencia hereditaria del factor VIII (FVIII) y afecta principalmente al sexo masculino. De acuerdo con la Federación mundial de Hemofilia, en Chile existen alrededor de 1.500 personas con hemofilia A (HA).1,2
El uso de concentrados de FVIII para el tratamiento y la profilaxis ha mejorado drásticamente el curso clínico de los pacientes con HA3. Sin embargo, existen pacientes que desarrollan anticuerpos contra el FVIII, lo cual dificulta el manejo de estos pacientes e impacta en los costos de tratamiento.
Emicizumab es un anticuerpo monoclonal para el tratamiento profiláctico de la hemofilia A en pacientes con y sin inhibidores del FVIII, que se une al factor IX y factor X, permitiendo restablecer la función hemostática. Emicizumab se administra por vía subcutánea y se dosifica de manera semanal, quincenal o mensual y ha demostrado tener una alta eficacia en los estudios clínicos de fase III 4.
El objetivo de este trabajo es determinar mediante un análisis farmacoeconómico la conveniencia médica y económica para el Fondo Nacional de Salud (Fonasa) de adoptar emicizumab como profilaxis para pacientes con hemofilia A. Para este análisis, durante el año 2019, se estimó el costo y la efectividad de emicizumab en comparación con las otras alternativas terapéuticas actualmente en uso en Chile, para adultos y niños con o sin inhibidores. Además, se realizó un análisis de impacto presupuestario, donde se calculan los costos, ahorros y se estima cuál será el aumento neto en el flujo de caja de asegurador o pagador.
El análisis demostró que el uso de emicizumab como profilaxis para la hemofilia A severa en niños y adultos es una estrategia costo-efectiva dominante debido a que disminuye los costos de los pacientes, entre 5 y 9 Millones de dólares a lo largo de su vida y, aumenta los años de vida ajustados por calidad (QALYs) de los pacientes.
Además, la adopción de profilaxis con Emicizumab resultaría en un importante ahorro neto para Fonasa, con un potencial de $6.187 millones de pesos chilenos ahorrados anualmente (US$ 8,79 millones).
Abstract
Hemophilia A is a pathology caused by an inherited factor VIII deficiency (FVIII) and mainly affects males. According to the World Federation of Hemophilia, in Chile there are around 1,500 people with hemophilia A (HA).
The use of FVIII concentrates for treatment and prophylaxis has dramatically improved the clinical course of patients with HA3. However, there are patients who develop antibodies against FVIII, which makes it difficult to manage these patients and increases treatment costs.
Emicizumab is a monoclonal antibody for the prophylactic treatment of hemophilia A in patients with and without FVIII inhibitors. It binds to both factor IX and factor X, restoring the lost hemostatic function of FVIII. Emicizumab is administered subcutaneously and is dosed weekly, every two weeks, or every four weeks. Also, emicizumab has been shown to be highly effective in phase III clinical trials.4
The objective of this study is to determine through a pharmacoeconomic analysis the medical and economic pros and cons for the National Health Fund (Fonasa) of adopting emicizumab as prophylaxis for patients with hemophilia A.
The analysis showed that the use of emicizumab as prophylaxis for severe hemophilia A in children and adults is a dominant cost-effective strategy because it reduces the costs of prevention and treatment of patients throughout their lives and increases their quality-adjusted life years (QALYs).
Furthermore, the adoption of prophylaxis with Emicizumab would result in significant net savings for Fonasa, with a potential of $ 6,187 million Chilean pesos saved annually (US$ 8.79 million).
Palabras claves
Hemofilia A, costo efectividad, Fonasa, impacto presupuestal, emicizumab
Introducción
La hemofilia es causada por una deficiencia hereditaria del factor de coagulación VIII o IX, correspondiendo a Hemofilia A o B, respectivamente, y afecta principalmente a hombres. La incidencia de la hemofilia A (HA) es de 1 caso cada 5.000 a 10.000 varones (85% de los casos de hemofilia), mientras que aquella de la hemofilia B es de 1 cada 30.000 varones (15% de los casos). Se estima que la prevalencia mundial es de alrededor de 440.000 personas. 5
El costo del manejo médico de la hemofilia se sitúa entre los más elevados de todas las enfermedades. En un estudio realizado en EE.UU. se estimó que en 2017 la hemofilia causó una carga de enfermedad de 110.095 años de vida ajustados por discapacidad (AVADS, o en inglés DALYs), equivalente a 0,33 DALYs por cada 1.000 habitantes. 6
El grado de deficiencia de factor determina la gravedad de la afección, definiéndose una enfermedad severa cuando los niveles de factor se encuentran por debajo del 1% de lo normal. Pacientes con enfermedad moderada (1%-5%) y aquellos con enfermedad leve (>5% a 40%).7 Para reducir el riesgo de hemorragias, a los pacientes con hemofilia A severa se les suele administrar concentrados de factor VIII (FVIII) por vía intravenosa varias veces por semana. Su uso ha mejorado drásticamente el tratamiento y el curso clínico de los pacientes con HA 6. Aproximadamente un tercio de los pacientes con hemofilia severa que reciben concentrados de FVIII desarrollan anticuerpos neutralizantes conocidos como inhibidores 4, convirtiéndose en la principal complicación del tratamiento. En estos pacientes la estrategia clínica tiene como objetivo la erradicación de inhibidores a través de la inmunotolerancia (ITI), sin embargo cuando éstos persisten, el manejo de los pacientes se realiza a través de terapias bypass 8.
Realidad local
En Chile, el año 2006 la hemofilia ingresó al Régimen de Garantías Explícitas en Salud como problema número 33 y su manejo se encuentra legalmente garantizado para el 100% de los pacientes en el país 9. El Ministerio de Salud de Chile (MINSAL) estimó que en el país existen 28,2 casos por cada 100.000 hombres beneficiarios en el Fondo Nacional de Salud (Fonasa) y 8,5 por 100.000 hombres beneficiarios de las Instituciones de Salud Previsional (Isapre), para una población total de aproximadamente 1.980 personas con la enfermedad 2. Actualmente, según la Federación Mundial de Hemofilia (FMH), en Chile habría alrededor de 1.500 personas que sufren de hemofilia A, con un número de 24 pacientes con inhibidores activos 2.
Emicizumab
Se han desarrollado avances en el área de hemofilia que han traído múltiples innovaciones tecnológicas que contribuyen al tratamiento de esta enfermedad, dentro de las cuales la primera en salir al mercado es emicizumab 10,11. Emicizumab es un anticuerpo monoclonal para el tratamiento profiláctico de la hemofilia A en pacientes con y sin inhibidores del FVIII, que se une al factor IX y factor X, para restablecer la función del FVIII faltante, permitiendo alcanzar un balance hemostático 10. Emicizumab se administra por vía subcutánea y se dosifica de manera semanal, quincenal o mensual 5, 12. En cuanto a su eficacia, en pacientes mayores de 12 años con hemofilia A con inhibidores, se demostró un 87% de reducción de sangrado tratados. Dos tercios de los pacientes en profilaxis con emicizumab estuvieron libres de sangrado en un año. Asimismo, en pacientes menores de 12 años con hemofilia A con inhibidores, el 77%, 90% y 60%, no sufrieron sangrados que tuvieran que ser tratados en las posologías semanal, quincenal y cada 4 semanas, respectivamente 13,14. En pacientes con hemofilia A sin inhibidores, se observó un 96% de reducción en los episodios de sangrado, con tasa anual de sangrado de 1,5, en comparación con 38 episodios en los pacientes sin profilaxis. Un 60% no tuvo sangrados.13,15
Si bien existen artículos publicados en Europa y en Estados Unidos que permiten estimar la relación de costo-efectividad del tratamiento con este anticuerpo monoclonal 16,17, en Chile no hay estudios que analicen el impacto de la incorporación de esta nueva tecnología. Por ello, el objetivo de este trabajo es determinar mediante un análisis farmacoeconómico la conveniencia médica y económica para el Fonasa de adoptar emicizumab como profilaxis para pacientes con hemofilia A.
Materiales y Métodos
Experiencia del paciente
La caracterización de la experiencia de los pacientes con hemofilia A severa (frecuencia de sangrados, hospitalizaciones, etc.) se basó en el conocimiento de expertas nacionales en hemofilia, pertenecientes al Hospital Roberto del Río, centro de referencia de hemofilia en Chile y al Hospital del Salvador.
Alternativas terapéuticas y las prácticas clínicas
Las dosis usadas en el manejo de la hemofilia en Chile son variables, por lo que no existe una práctica única o de consenso. Es por eso por lo que en todos los casos este estudio se basó en la opinión del panel de expertas. Sin embargo, puesto que en Chile prácticamente no hay experiencia en el uso de emicizumab, los parámetros sobre prácticas clínicas para este nuevo fármaco fueron extraídos de los estudios Haven 1 y 2 13,15, con una dosis de carga de 3 mg/kg a la semana por 4 semanas, seguido de 1.5 mg/kg semanal.
Para este informe solamente se trabajará con la profilaxis y tratamiento de pacientes con hemofilia tipo A severos con inhibidores.
Costos médicos y financiamiento
El panel de expertas definió los tipos de profilaxis, dosis, cantidad de sangrados y tipos de tratamientos de los pacientes con HA severa según experiencia en terreno y literatura internacional. Estas dosis de profilaxis y tratamientos se multiplicaron por el precio (incluyendo el Impuesto al Valor Agregado, IVA, del 19%) de cada una de las unidades de administración según muestra la Tabla 1.
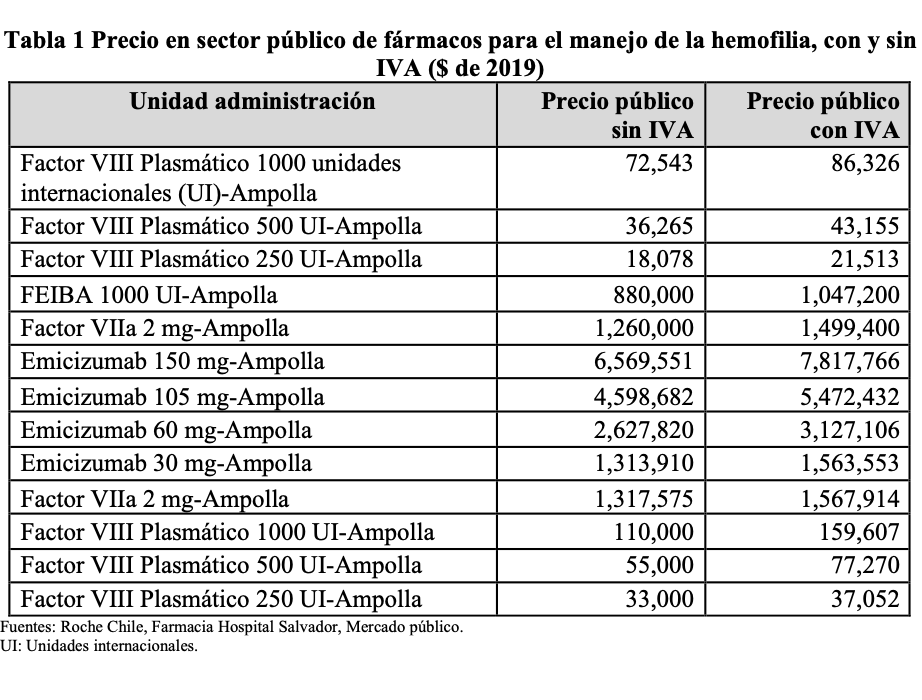
Análisis de costo-efectividad
Para este análisis se estimó el costo y la efectividad de emicizumab en comparación con las otras alternativas terapéuticas actualmente en uso en Chile, para adultos y niños con o sin inhibidores, incluyendo: (1) sin profilaxis, (2) profilaxis con agentes bypass (3) profilaxis con rFVIIa. En todos los casos se supuso que los pacientes son tratados con agentes bypass durante un episodio de sangrado. Para los costos, los resultados fueron expresados en pesos chilenos y dólares americanos (US); y para la efectividad, en años de vida ajustados por calidad (QALYs). Tanto costos como efectividad en años futuros fueron actualizados a valor presente, usando una tasa de descuento real anual del 3%.
Los autores calcularon los costos anuales para los distintos tipos de pacientes y los diferentes estados. Los costos se dividieron en profilaxis más ITI, costos de sangrado leve y costos de sangrado grave. Para los costos de profilaxis, en el caso de adultos y niños, se consideraron distintos escenarios para el precio de Emicizumab. Para los dos últimos estados, se ponderó por tipo de tratamiento y se incluyeron los costos adicionales de días camas, exámenes y consultas médicas de seguimiento.
Para realizar el análisis de costo-efectividad se utilizó un modelo de Markov, donde se utilizó un diagrama de transición como el que se muestra en la Figura 1. Este diagrama muestra cómo un paciente sin sangrado puede transitar entre un ciclo semanal (frecuencia que captura adecuadamente las variaciones habituales en el estado de salud de pacientes con hemofilia) y el siguiente a otros estados: sangrado leve, sangrado severo y muerte.
Figura 1 Diagrama de transición pacientes con hemofilia A severos
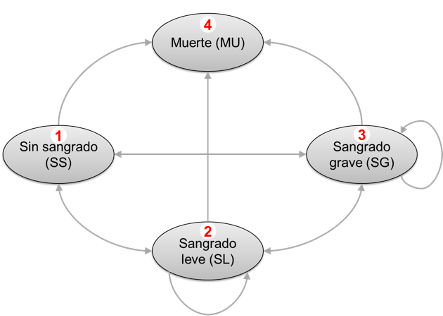
Fuente: Elaboración propia.
Cada uno de estos estados tiene asociado un costo y una efectividad. El costo incluye el de la profilaxis y del tratamiento de los sangrados y fue medido en pesos chilenos. Los costos fueron calculados por los autores usando la información recabada sobre la realidad chilena, con la ayuda del panel de expertas. La efectividad fue formulada como el nivel de salud del paciente correspondiente a cada estado y fue medida en QALYs. Los valores para la efectividad, por su parte, fueron obtenidos del único estudio disponible en la literatura, realizado por ICER y que, como este, evalúa la relación de costo efectividad del uso de emicizumab en pacientes con hemofilia A severa.16 Esta información se presenta en la siguiente tabla. En el modelo estas utilidades anuales fueron transformadas a utilidades semanales para ser consistentes con la duración de los ciclos aquí definidos.
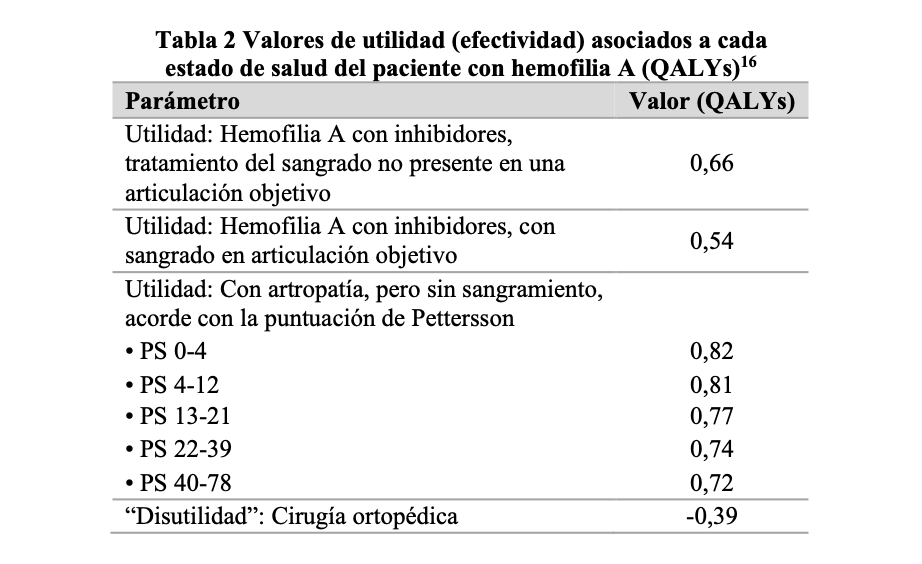
Considerando que uno de los estados de salud posibles del paciente es la muerte, fue necesario usar una tabla de mortalidad (figura 2), con la tasa de mortalidad anual que se utilizó en los pacientes con hemofilia según grupo etario. Esta información fue obtenida de la literatura internacional, por falta de literatura nacional al respecto.
Figura 2 Edad del paciente y horizonte temporal en el modelo de Markov 17

Fuente: Elaboración propia.
- 1.1. Análisis de impacto presupuestario
El análisis de impacto presupuestario calcula los costos, ahorros y estima cuál será el aumento neto en el flujo de caja de asegurador o pagador. Los gastos de operación dependerán de la cantidad de individuos o pacientes que se tratarán con la nueva tecnología y de la cantidad y el costo de los insumos que esta requiera por paciente.
Para los cálculos de dosis se utilizó como referencia un adulto de peso de 70Kg y un niño de 35 Kg. La dosis se redondeó a la más cercana según los viales actuales. Dado que en Chile no hay experiencia con emicizumab, estos datos fueron extraídos de los estudios HAVEN 1, 2 y 3, que constituyen la referencia internacional para este fármaco.
Las dosis de evento de sangrados con agentes bypass se extrapolaron desde las dosis recomendadas para cirugía menor contenidas en las Guías MINSAL 2013.
Debido a que en niños el rFVIIa tiene vida media más corta, en ellos la dosis inicial en eventos de sangrado calculada fue 120 ug/Kg, a diferencia de adultos en que la dosis inicial calculada fue con 90mc/Kg.
Se incluyó el escenario de pacientes en profilaxis con Emicizumab e ITI, a pesar de que no existe ningún dato a la fecha sobre esta combinación. Sin embargo, se asumió que, dada la aplicabilidad de emicizumab, este será un escenario posible en el futuro.
Respecto a la ITI, existen varios esquemas, incluyendo: 50 UI/Kg, 3 veces por semana y otros de 100-200 UI/kg día. Estos esquemas se usan por al menos 2 años. El esquema se decide según varios criterios, como los siguientes: accesos venosos, cercanía con el centro de tratamiento, factores de riesgo para mala respuesta, clínica para el tratamiento de hemorragias del paciente, etc. En el análisis se supuso 100 UI/Kg /día, ya que es lo más descrito en la literatura.
La ITI se usa concomitantemente con profilaxis (complejo protrombínico activado o rFVIIa) durante 1 año en pacientes con fenotipo hemorrágico hasta que el paciente “inmuno-tolere”. Por ello en el caso de los niños se contempló dos escenarios: con y sin ITI más profilaxis con agentes bypass.
Resultados
Experiencia del paciente, alternativas terapéuticas y prácticas clínicas
El panel de expertas consensuó que para la profilaxis de la hemofilia en Chile se utilizan distintas alternativas terapéuticas que dependen de decisiones médicas y presupuestarias. A continuación, se presentan las alternativas terapéuticas para niños y adultos, con y sin inhibidores:
Figura 3 Alternativas de tratamiento profilaxis Hemofilia A en adultos y niños
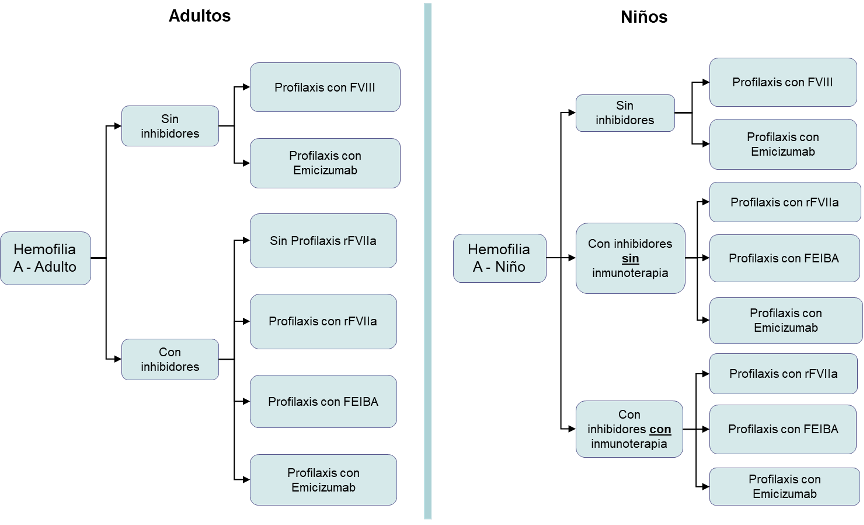
Fuente: Elaboración propia
Esquemas terapéuticos
En consulta con expertas durante el estudio, se convino que las dosis usadas para el tratamiento de los sangrados en pacientes con hemofilia son variables, por lo que en todos los casos se usó una estimación basada en el sangrado más frecuente y en su duración promedio; esto es, hemartrosis, durante 5 días. A continuación se presenta en forma tabular un resumen de los esquemas terapéuticos donde en las filas corresponden a los tipos de tratamiento por paciente y las columnas a las dosis de profilaxis y las de sangrados. Estas últimas están separadas según dosis internacionales y dosis que se usaron en el estudio.
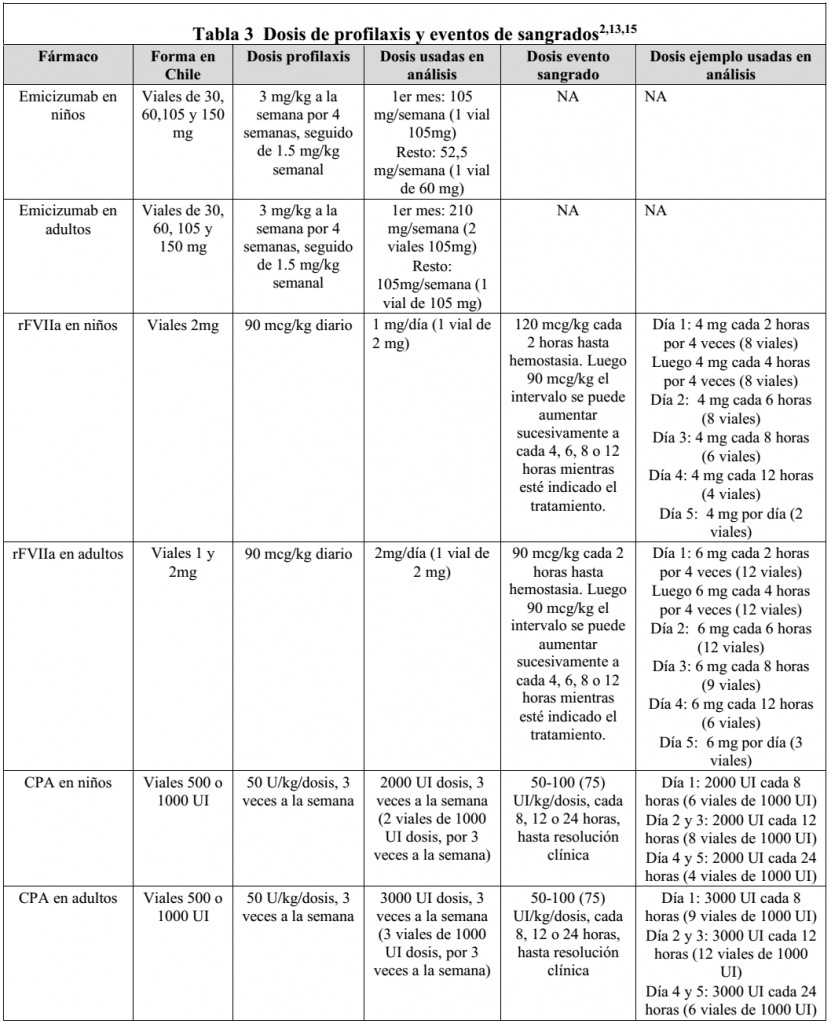
CPA: complejo protrombínico activado
Fuente: Elaboración propia.
Adicionalmente, se estimó la cantidad de sangrados según los diferentes escenarios de profilaxis en hemofilia A severa con inhibidores. En la Tabla 4 se detalla en las filas la cantidad de sangrados por tipo de profilaxis y en las columnas la tasa de sangrado según los estudios internacionales, sus fuentes y los sangrados estimados por los expertos.
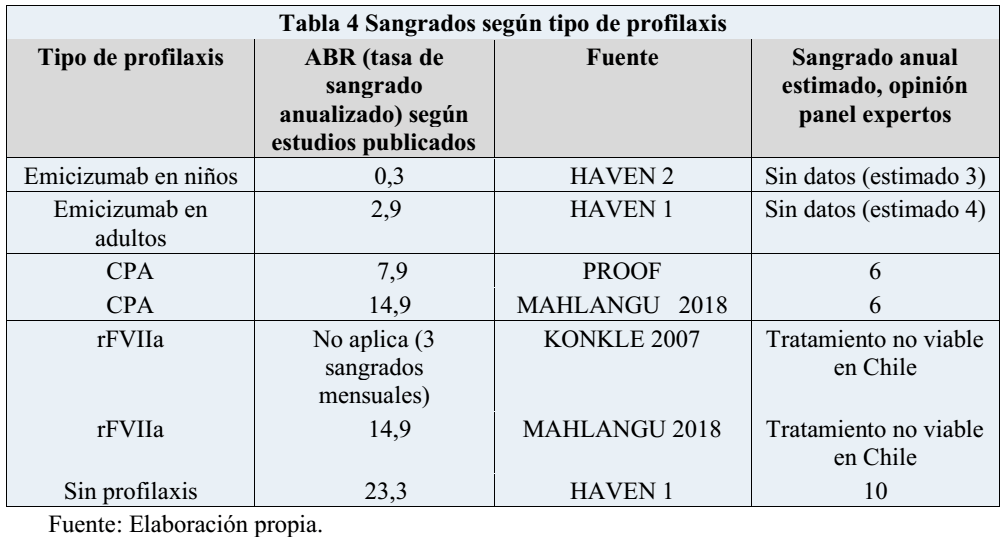
Según las alternativas terapéuticas y las prácticas clínicas recién descritas, se calculó el costo de la profilaxis y tratamientos de sangrados para adultos y niños, con y sin inhibidores.
Resultados del análisis de costo-efectividad de la profilaxis con emicizumab en adultos y niños con inhibidores
El principal resultado de este trabajo es que emicizumab es una estrategia dominante ante cualquiera de las otras alternativas de profilaxis en adultos y niños con inhibidores (con y sin ITI) (ver Tabla 5).
La columna “Costo” contiene el valor presente del costo en dólares (US) asociado a cada grupo de paciente y cada estrategia de manejo. Estos costos se presentan por paciente, no para la totalidad de los pacientes que existen en Chile. Es decir, se trata de todos los costos futuros asociados a la profilaxis (de haberla) y al tratamiento de un paciente, durante la cantidad de años futuros que corresponda.
Como se detalla en la tabla 5, el menor costo y la estrategia más eficaz en el manejo del paciente con hemofilia corresponde a la estrategia en la que se usa emicizumab
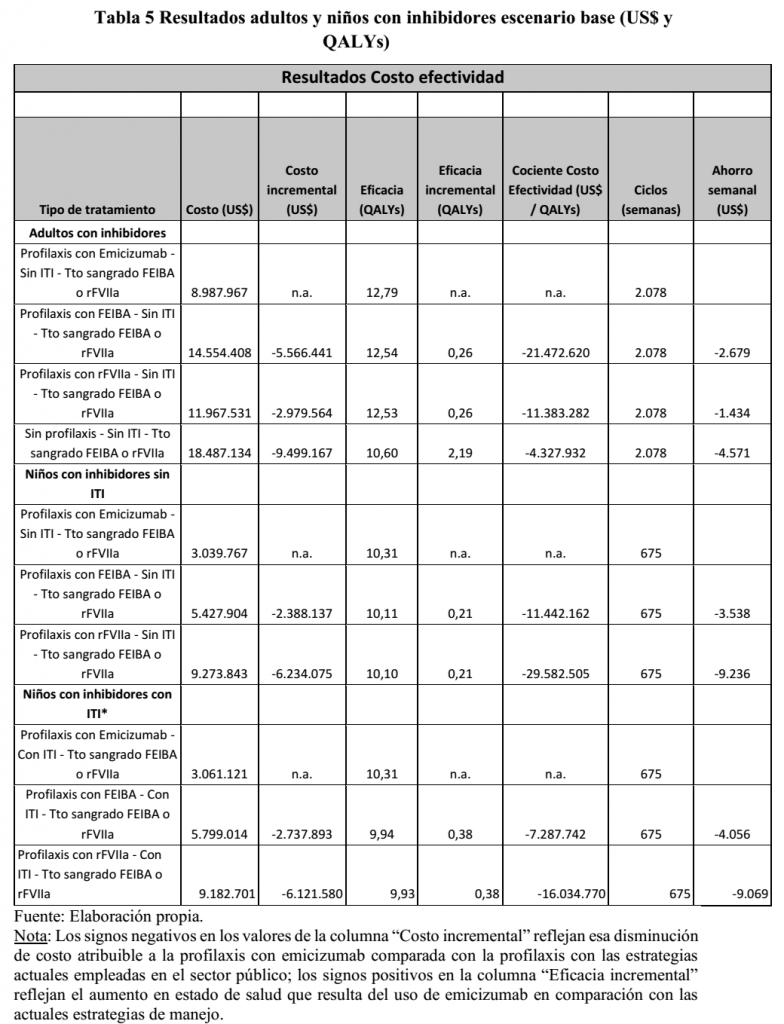
Resultados del análisis de impacto presupuestario
La adopción de profilaxis con emicizumab resultaría en un importante ahorro neto para Fonasa. Es decir, el impacto presupuestario de esta medida sería favorable. En efecto, si la profilaxis de los 28 pacientes niños y adultos que sufren de hemofilia A severa con inhibidores fuese con emicizumab, ello le significaría a Fonasa un ahorro neto anual de $4.574 Millones CLP.
Tabla 6 resultados Impacto presupuestario niños y adultos con HA con inhibidores
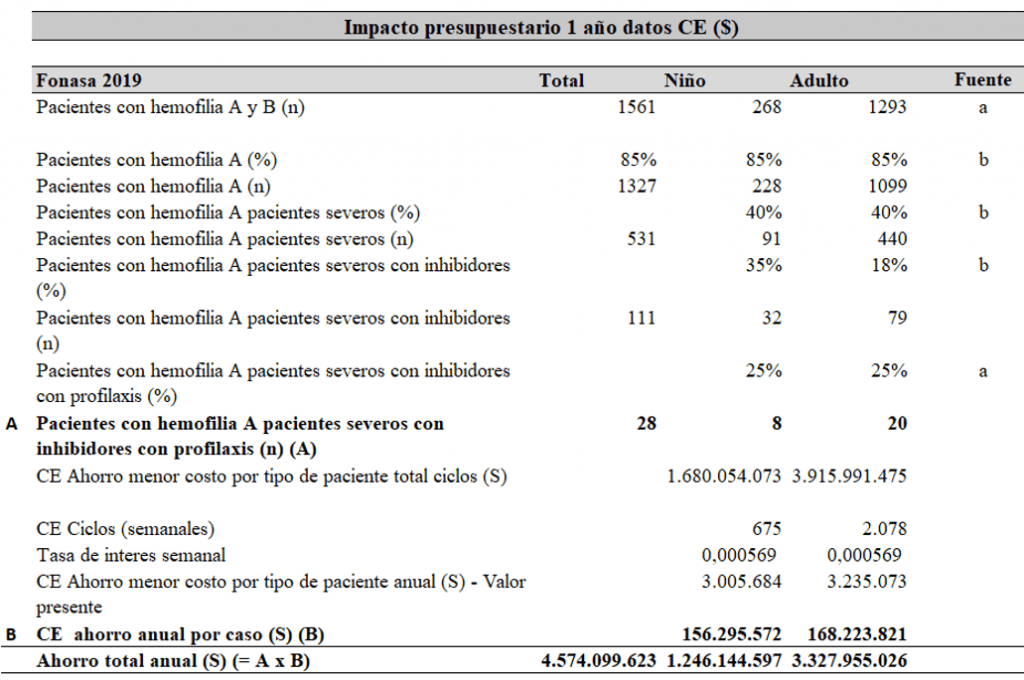
a. Minsal 2019, Informe final del EVC 2018 – DEMANDA.
b. Panel de expertas.
c. Flujos descontados con una tasa del 10% real anual.
Discusión
Existen estudios internacionales que presentan a emicizumab como una alternativa costo-efectiva y eficaz para el tratamiento de personas con HA con inhibidores 17,18.
En esa misma línea, expertos clínicos se han preguntado si esta terapia es accesible y alcanzable para la gran comunidad global de la hemofilia. Al igual que en otros estudios, para corroborar el diseño del modelo y datos importantes que permitieron el análisis en el estudio en Chile, los autores solicitaron la opinión de expertas para llenar los vacíos en las estimaciones de los parámetros. Esto incluyó la proporción de pacientes con inhibidores y la de pacientes con inhibidores que se encuentran en ITI, además de la proporción personas con HA tratadas con rFVIIa y aPCC. Un estudio en Italia recientemente publicado demostró, como lo hizo este trabajo en Chile, que emicizumab genera ahorros significativos en comparación con agentes bypass en el costo de los medicamentos usados para pacientes con hemofilia A con inhibidores 19.
El análisis aquí presentado ha demostrado para el caso del sector público en Chile que el uso de emicizumab como profilaxis para la hemofilia A severa en niños, adolescentes y adultos es una estrategia costo-efectiva dominante. Esto se explica por dos fenómenos. Primero, este anticuerpo monoclonal disminuye los costos de prevención y tratamiento de los pacientes a lo largo de su vida. Segundo, la profilaxis con emicizumab ha demostrado tener mayor eficacia que los tratamientos actuales para los pacientes chilenos con HA e inhibidores: emicizumab aumenta los años de vida ajustados por calidad de los pacientes. La característica dominante de la profilaxis con emicizumab se grafica a continuación.
Figura 4 Interpretación de los resultados de este estudio de costo-efectividad del uso de Emicizumab como profilaxis de la hemofilia en niños y adultos con inhibidores.
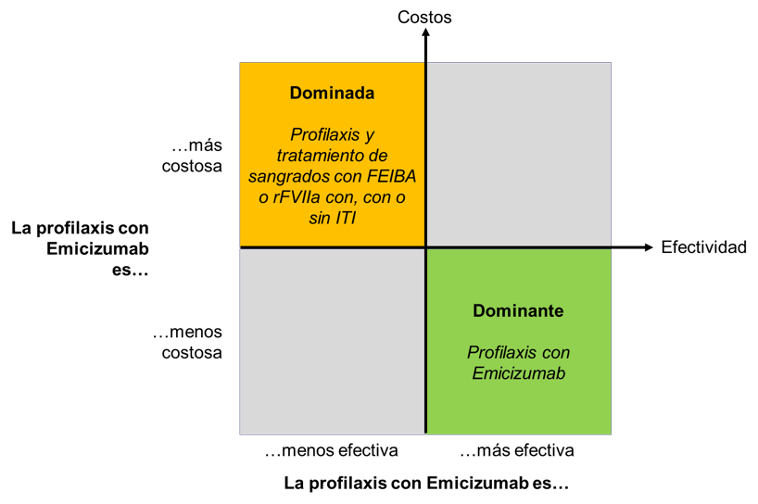
Fuente: Elaboración propia.
Si se realiza una sensibilización (simulación) en donde se puede hacer profilaxis con rFVIIa y la cantidad de sangrados varía según criterio de experto, Emicizumab como profilaxis para la hemofilia A severa en niños y adultos sigue siendo una estrategia costo-efectiva dominante.
En la actualidad hay pacientes niños y adultos en tratamiento con ITI y sin profilaxis, situación que se debe reflejar en los cálculos de impacto presupuestario. Sin embargo, se desconoce su número, por lo que no es posible cuantificar de manera cierta el impacto presupuestario para Fonasa asociado al uso de Emicizumab.
Por último, a la luz de la conveniencia para pacientes de Fonasa con inhibidores de usar emicizumab como profilaxis, es recomendable examinar también el potencial uso equivalente de este medicamento en pacientes sin inhibidores.
Limitaciones de este estudio
Como se dijo al inicio de este documento, en Chile no existe una norma ni una práctica uniforme en los sectores público y privado respecto de las dosis usadas en el manejo de la hemofilia. Los autores caracterizaron y costearon las actuales prácticas respecto al uso de Factor VIIa y FEIBA basándose en la información proporcionada por un panel de expertas. Por otra parte, como también se dijo, la experiencia en Chile con el uso de emicizumab es muy limitada, pues se refiere a solo unos pocos pacientes. Por ello, los autores no pudieron usar información nacional sobre prácticas en el uso de este nuevo fármaco, sino que prefirieron adoptar las prácticas reportadas en los estudios Haven 1 y 2. No obstante, los autores concluyeron que los resultados del estudio de costo-efectividad presentado son robustos y que no cambian la principal conclusión del trabajo al variar en rangos razonables los parámetros que caracterizan las prácticas actuales de uso de fármacos o las prácticas futuras que se pudieran establecer en Chile para el uso de emicizumab.
Conclusión.
Este análisis ha demostrado que el uso de emicizumab como profilaxis para la hemofilia A grave en niños y adultos es una estrategia costo-efectiva dominante. Además, la adopción de profilaxis con Emicizumab resultaría en un importante ahorro neto para Fonasa.
Agradecimientos
Los autores de este estudio agradecen a las siguientes expertas nacionales en hematología por su ayuda en la definición de prácticas clínicas y de respuesta a terapias alternativas de los pacientes hemofílicos en el sector público chileno:
- Dra. Verónica Soto, Hematóloga, Hospital Roberto del Río
- Dra. Daniela Cortéz, Hematóloga, Hospital Roberto del Río
- Dra. Ximena Valladares, Hematóloga, Hospital del Salvador
También agradecen a los participantes en el taller de consulta realizado el 16 de octubre de 2019 en el Hotel Regal Pacific, durante el cual los autores presentaron y recibieron comentarios sobre sus métodos, supuestos y resultados preliminares.
No obstante, cualquier error u omisión de este informe es de exclusiva responsabilidad de los autores.
Referencias.
- Ministerio de Salud (2013). Guía Clínica AUGE Hemofilia 2013. Serie Guías Clínicas MINSAL. Consultado en https://diprece.minsal.cl/wrdprss_minsal/wp-content/uploads/2014/12/Hemofilia.pdf
- Ministerio de Salud (2009). Informe Final. Estudio Verificación del Costo Esperado Individual Promedio por Beneficiario del Conjunto Priorizado de Problemas de Salud con Garantías Explícitas – 2009
- Kempton, C. L. and S. L. Meeks (2014). «Toward optimal therapy for inhibitors in hemophilia.» Blood 124(23): 3365-3372.
- Folleto de información al profesional Hemlibra CDS 2.0. 2018. Consultado en https://www.roche.cl/content/dam/rochexx/roche-cl/documents/folletos/Folleto%20Medico%20Hemlibra%20CDS%202.0%20a%205.0%20(oct%202018).pdf
- ¿Qué es la hemofilia? Hemofilia en Chile (s.f). Sociedad chilena de la hemofilia. Consultado en https://hemofiliaenchile.cl/que-es-la-hemofilia/
- Institute for Clinical and Economic Review (2017). «Emicizumab for Hemophilia A: Effectiveness and Value. Final Background and Scope. Consultado en https://icer-review.org/wp-content/uploads/2017/08/NECEPAC_Hemophilia_Revised_Scope_101017.pdf
- Estimación de los autores basada en: (a) Siddiqi, A. E., et al. (2010). «Burden of disease resulting from hemophilia in the U.S.»
- Ozelo MC, Villaça PR, Pérez-Bianco R, Candela M, Garcia-Chavez J, Moreno-Rodriguez B, et al. (2014) Musculoskeletal evaluation in severe haemophilia A patients from Latin America. Haemophilia. Jan;20(1): e63-70.
- Donoso M. (2013) Hemofilia en Chile: 1996-2006. Medwave;13(5): e571
- Peters, R., & Harris, T. (2018). Advances and innovations in haemophilia treatment. Nature Reviews Drug Discovery, 17(7), 493-508.
- Callaghan, M. U., Sidonio, R., & Pipe, S. W. (2018). Novel therapeutics for hemophilia and other bleeding disorders. Blood, 132(1), 23-30.
- O’Hara, J., Sima, C. S., Frimpter, J., Paliargues, F., Chu, P., & Presch, I. (2018). Long‐term outcomes from prophylactic or episodic treatment of haemophilia A: A systematic review. Haemophilia, 24(5), e301-e311.
- Oldenburg J, Mahlangu JN, Kim B, Schmitt C, Callaghan MU, Young G, et al. Emicizumab Prophylaxis in Hemophilia A with Inhibitors. N Engl J Med. 2017;377:809–18.
- Mahlangu, J. (2019). Emicizumab for the prevention of bleeds in hemophilia A. Expert opinion on biological therapy, 19(8), 753-761.
- Young G, Liesner R, Chang T, et al. A multicenter, open-label phase 3 study of emicizumab prophylaxis in children with hemophilia A with inhibitors. Blood. 2019;134(24):2127‐2138. doi:10.1182/blood.2019001869
- Institute for Clinical and Economic Review (2018). Emicizumab for Hemophilia A with Inhibitors: Effectiveness and Value. Consultado en https://icer-review.org/wp-content/uploads/2017/08/ICER_Hemophilia_Final_Evidence_Report_041618.pdf
- Darby et all (2019) Mortality rates, life expectancy, and causes of death in people with hemophilia A or B in the United Kingdom who were not infected with HIV
- Patel, A. M., Corman, S. L., Chaplin, S., Raimundo, K., & Sidonio, R. F. (2019). Economic impact model of delayed inhibitor development in patients with hemophilia a receiving emicizumab for the prevention of bleeding events. Journal of medical economics, 22(12), 1328-1337.
- Cortesi PA, Castaman G, Trifiró G, et al. (2020). Cost effectiveness and Budget Impact of Emicizumab Prophylaxis in Haemophilia A patients with inhibitors. Coagulation and Fibrinolysis, 120(02): 216-228.













